Uvod u proizvod
| Tetrabutilamonijev bromid Osnovne informacije |
| Fizikalna i kemijska svojstva Primjena Koristi pripravak Toksičnost |
| Ime proizvoda: | Tetrabutilamonijev bromid |
| Sinonimi: | 1-Butanaminij, N,N,N-tributil-,bromid;1-Butanaminij,N,N,N-tributil-,bromid;n,n,n-tributil-1-butanaminiubromid; ALIQUAT(R) 100;IPC-TBA-BR;Tetrabutilazanijev bromid;Tetrabutilaminijev·bromid;Tetrabutilamonijev bromid, 99%, za kromatografiju ionskih parova |
| CAS: | 1643-19-2 |
| MF: | C16H36BrN |
| MW: | 322.37 |
| EINECS: | 216-699-2 |
| Kategorije proizvoda: | organo amin halid; ostali proizvodi; amonijeve soli esencijalne kemikalije; reagens plus; rutinski reagensi; amonijeve soli analitički reagensi; elektrokemija; pomoćni elektroliti za elektrokemiju; anionski HPLC; kromatografija/CE reagensi; ionski par; reagensi za ionske parove; s - anionski; ionski par Reagensi - anionski koncentrat; kvarterne amonijeve soli; amonijevi bromidi (kvaternarni); analitička kemija; HPLC reagensi za ionske parove za kisele uzorke; reagensi za ionske parove za HPLC; kvarterni amonijevi spojevi; amonijeve, fosfonijeve, sulfonijeve soli (ionske tekućine); ionske Tekućine;Sintetička organska kemija;Amonijeve soli;Ekološkije alternative: kataliza;Katalizatori faznog prijenosa;Farmaceutski intermedijeri;1643-19-2;bc0001 |
| Mol datoteka: | 1643-19-2.mol |
 |
|
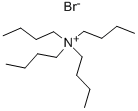
| Tetrabutilamonijev bromid Kemijska svojstva |
| Talište | 102-106 stupanj (lit.) |
| Vrelište | 102 stupnja |
| gustoća | 1,039 g/mL na 25 stupnjeva |
| tlak pare | 0Pa na 25 stupnjeva |
| indeks loma | n20/D 1.422 |
| Fp | 100 stupnjeva |
| temp. skladištenja | Čuvati ispod +30 stupnjeva. |
| topljivost | H2O: 0.1 g/mL, bistro, bezbojno |
| oblik | Kristalni prah |
| pka | 0[na 20 stupnjeva] |
| Specifična gravitacija | 1.007 |
| boja | Bijelo do blago kremasto |
| Miris | Amin poput |
| PH | 3,5 do 7.0 (50 g/L, 25 stupnjeva) |
| Topljivost u vodi | 600 g/L (20 ºC) |
| Osjetljiv | Higroskopno |
| λmaks | λ: 240 nm Max: 0,04 λ: 250 nm Amax: 0,03 λ: 260 nm Amax: 0,02 λ: 500 nm Max: 0,02 |
| BRN | 3570983 |
| Stabilnost: | Stabilan. Nekompatibilno s jakim oksidirajućim sredstvima. Zaštititi od vlage. |
| InChIKey | JRMUNVKIHCOMHV-UHFFFAOYSA-M |
| LogP | 0.839 na 25 stupnjeva |
| CAS Referenca baze podataka | 1643-19-2(CAS referenca baze podataka) |
| NIST kemijska referenca | Tetra-N-butilamonijev bromid (1643-19-2) |
| Sustav registra tvari EPA | Tetrabutilamonijev bromid (1643-19-2) |
| Sigurnosne informacije |
| Šifre opasnosti | Xi, Xn |
| Izjave o riziku | 36/37/38-22 |
| Izjave o sigurnosti | 26-36-37/39 |
| WGK Njemačka | 3 |
| F | 3 |
| Napomena o opasnosti | Nadražujuće |
| TSCA | Da |
| HS kod | 29239000 |
| MSDS informacije |
| Davatelj | Jezik |
|---|---|
| Tetrabutilamonijev bromid | Engleski |
| ACROS | Engleski |
| SigmaAldrich | Engleski |
| ALFA | Engleski |
| Upotreba i sinteza tetrabutilamonijevog bromida |
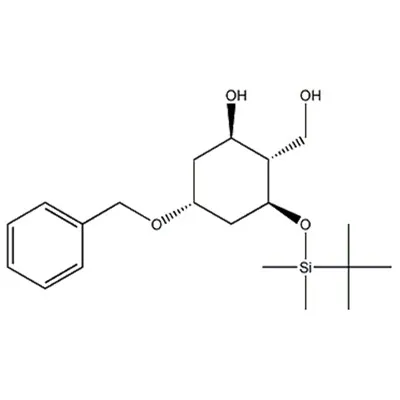
| Fizička i kemijska svojstva | Tetrabutilamonijev bromid, poznat i kao tetrabutilamonijev bromid. Bijeli kristal, rasplinjavanje. 118 stupnjeva tališta. Topljiv u vodi, alkoholu, eteru i acetonu, slabo topljiv u benzenu.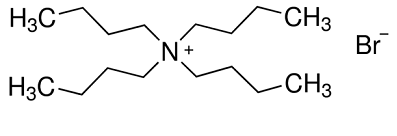 Slika 1: strukturna formula tetrabutilamonijevog bromida |
| Primjena | (1) Koristi se kao reagens za analizu organske sinteze. (2) Tetrabutilamonijev bromid također je učinkovit katalizator faznog prijenosa. Katalizator faznog prijenosa, koji se naziva PTC, može prenijeti vodenu fazu (ili organsku fazu) u organsku fazu (ili vodenu fazu) katalizatora, što može dovesti do reakcije između vodene faze i organske faze katalizatora. PTC ima funkciju mijenjanja stupnja solvatacije iona, povećanja aktivnosti ionske reakcije, ubrzavanja brzine reakcije i tako dalje. Riješite problem prošlosti u dvije faze reakcije je teško reagirati. Uobičajeni katalizatori faznog prijenosa kvaterne amonijeve soli su: benzil trietil amonijev klorid, trioktil metil amonijev klorid, tetrametil amonijev bromid, tetrapropilamonijev klorid, tetrabutilamonijev bromid, tetrabutil amonijev jodid, benzil trietil amonijev bromid, trietil heksil bromid, oktil trietilamonijev bromid mide. Katalizator faznog prijenosa naširoko se primjenjuje u organskoj sintezi: R2C za pripremu spojeva (spoj tipa karbena), daljnju pripremu odgovarajućeg nitrila, izonitrila, halona, diklorometana, ciklopropanskih derivata, hidroksi kiselina i diazometana. Za reakciju alkilacije, u usporedbi s tradicionalnim metodama, kako bi se izbjegli teški uvjeti suhog rada i visokog prinosa, također se može koristiti u redoks reakciji, hidrolizi estera, reakciji supstitucije, reakciji kondenzacije, reakciji dodavanja, reakciji polimerizacije, reakciji dodavanja ugljika i eliminacija reakcije i tako dalje. (3) Za intermedijere organske sinteze, katalizator faznog prijenosa (4) Reagensi za uparivanje iona za sintezu bakampicilina, sličnog sultamicilinu. (5) Reagensi za kromatografiju ionskih parova, katalizator faznog prijenosa. Bakampicilin, sinteza slična sultamicilinu. |
| Koristi | Tetrabutilamonijev bromid (TBAB) je kvaterni amonijev spoj. To je najrašireniji katalizator faznog prijenosa. Njegova međupovršinska svojstva proučavana su u slučaju reakcija iniciranih hidroksidom. Ovo se može primijeniti u razumijevanju mehanizma reakcija faznog prijenosa. Za TBAB se navodi da smanjuje vrijeme zadržavanja i uklanja vršne ostatke djelujući kao reagens ionskog para tijekom kromatografske analize kvaternih amonijevih spojeva. U rastaljenom stanju TBAB se ponaša kao ionska tekućina koja je obećavajuća zelena alternativa organskim otapalima u organskoj sintezi. Određeni su njegov molarni toplinski kapacitet, entropija i funkcija slobodne energije. Nedavno je rastaljeni tetrabutilamonijev bromid (TBAB) korišten kao nisko toksičan i isplativ IL u nizu konstruktivnih sintetskih transformacija. Tetrabutilamonijev bromid (TBAB) može se koristiti u rastaljenom stanju u sljedećim procesima: Sinteza (2S)-5-(3-fenil-2-ftalimidilpropanoilamino)izoftalne kiseline. Sinteza alkil-supstituiranih pirola u odsutnosti katalizatora i organskog otapala. Sinteza ditioacetala iz acetala transtioacetalizacijom u okruženju bez otapala. Sinteza poliamida (PA) polimerizacijom tereftalne kiseline i diizocijanata. Katalizirati adiciju tiola na konjugirane alkene. Dehidrokloriranje poli(vinil klorida). |
| priprema | Preparativne metode: dostupno je nekoliko metoda za učinkovito obnavljanje kvaternarnog amonijevog iona. Pripremljeno reakcijom tri-n-butilamina i n-butil bromida. |
| Toksičnost | Akutni oralni LD50 (miš): 590 mg/kg. Udisanje, gutanje i dodir s kožom otrovno za kožu, oči i iritaciju dišnog sustava. Više informacija od urednika ChemicalBook Xiaonan (2015-09-16). |
| Kemijska svojstva | bijeli kristali ili prah |
| Koristi | Tetrabutilamonijev bromid koristi se u sintezi polimernih solarnih ćelija. Također se koristi u sintezi jednokomponentnih elektrokemijskih ćelija koje emitiraju zeleno svjetlo. |
| Definicija | ChEBI: Tetrabutilamonijev bromid je tetrabutilamonijeva sol s bromidom kao anionskim dvojnikom. To je organska bromidna sol i tetrabutilamonijeva sol. |
| koristi | Tetrabutilamonijev bromid je ekološki benigna, nehlapljiva, nezapaljiva, nekorozivna, jeftina, komercijalno dostupna amonijeva sol visoke toplinske i kemijske stabilnosti. U TBAB-u, tetrabutilamonijeva sol može se otopiti iu vodenim iu organskim otapalima, što pomaže transportu anionskih reaktanata topivih u vodi u organsku fazu. Štoviše, rastaljeni TBAB također je korišten kao učinkovita ionska tekućina za izvođenje organskih transformacija u uvjetima bez otapala[1]. |
| Opći opis | Tetrabutilamonijev bromid, kvaterni amonijev spoj koji se široko koristi kao katalizator faznog prijenosa. TBAB smanjuje vrijeme zadržavanja i uklanja vršne ostatke djelujući kao reagens ionskog para tijekom kromatografske analize kvaternih amonijevih spojeva. U rastaljenom stanju, TBAB se ponaša kao ionska tekućina, što je obećavajuća zelena alternativa organskim otapalima u sintezi polimera. |
| Zapaljivost i eksplozivnost | Nije klasificirano |
| Metode pročišćavanja | Kristalizirajte sol iz *benzena (5mL/g) na 80o dodavanjem vrućeg n-heksana (tri volumena) i ostavite da se ohladi. Osušite preko P2O5 ili Mg(ClO4)2, pod vakuumom. Sol je vrlo higroskopna. Također se može kristalizirati iz etil acetata ili suhog acetona dodavanjem dietil etera i sušenjem u vakuumu na 60° 2 dana. Kristaliziran je iz acetona dodatkom dietil etera. Toliko je higroskopan da se sve manipulacije trebaju provoditi u suhoj kutiji. Pročišćen je taloženjem iz zasićene otopine u suhom CCl4 dodatkom cikloheksana ili rekristalizacijom iz etil acetata, zatim zagrijavanjem u vakuumu do 75° u prisutnosti P2O5. [Symons et al. J Chem Soc, Faraday Trans 1 76 2251 1908.] Također se rekristalizira iz CH2Cl2/dietil etera i suši u vakuumskom eksikatoru iznad P2O5. [Blau & Espenson J Am Chem Soc 108 1962 1986, Beilstein 4 IV 657.] |
| Reference | [1] Banik B, et al. Tetrabutilamonijevim bromidom (TBAB) katalizirana sinteza bioaktivnih heterocikla. Molekule, 2020.; 25: 5918. |
| Proizvodi i sirovine za pripremu tetrabutilamonijevog bromida |
| Proizvodi za pripremu | 1-BENZOTHIOPHENE-5-CARBOXYLIC ACID-->Albendazole-->Piperonyl aldehyde-->3-AMINOBIPHENYL-->5-Bromoindazole-->ETHYL 4-ETHOXYPHENYLACETATE-->H-GLY-AMC HBR-->1-Phenylcyclopentanecarboxylic acid-->3-PHENYLBENZYLAMINE-->4-PYRIDIN-2-YLISOXAZOL-5-AMINE-->cintofen-->FENOTHIOCARB-->(R)-(-)-2,2-Dimethyl-1,3-dioxolane-4-methanol-->Isocarbophos-->Venlafaxine hydrochloride-->1-BENZOTHIOPHENE-5-CARBONITRILE-->N-(4-THIOPHEN-2-YL-PHENYL)-ACETAMIDE-->Thianaphthene-2-carboxylic acid-->Myclobutanil-->alpha-butyl-alpha-phenyl-1H-imidazole-1-propiononitrile-->5-Bromobenzo[c]thiophene-->Olaquindox-->Sisthsne-->2-[2-(DIPHENYLPHOSPHINO)ETHYL]PYRIDINE-->Glyceryl monostearate-->1-(3-Aminopropyl)piperidine-->Phenyl vinyl sulfone-->6-Bromopurine-->Methyl 3,4,5-trimethoxybenzoate-->CYCLANILIDE-->2-(4-ETHOXYPHENYL)-2-METHYL PROPIONITRILE-->Levetiracetam-->4-Bromo-7-azaindole-->DIOCTYL ETHER-->1,1-Cyclopropanedicarboxylic acid dimethyl ester-->2 -phenyl-Hexanenitrile-->Zeolite-->Tetrabutylammonium hexafluorophosphate-->4-(tert-Butyl)benzyl mercaptan-->Tetrabutilamonijev borohidrid |
Popularni tagovi: tetrabutilamonijev bromid, Kina tetrabutilamonijev bromid proizvođači, dobavljači, tvornica
Mogli biste i voljeti
Pošaljite upit