
Uvod u proizvod
| Aluminijev fluorid Osnovne informacije |
| Opis Sinteza Primjena Toksikološke studije Sigurnost Reference |
| Naziv proizvoda: | Aluminijev fluorid |
| Sinonimi: | fluoridnost;ALUMINIJ TRIFLUORID;ALUMINIJ FLUORID;Aluminijev trifluorid;ALUMINIJ FLUORID;ALUMINIJ(III) FLUORID;Aluminijev fluorid,99.9+%, čist;ALUMINIJ FLUORID H |
| CAS: | 7784-18-1 |
| MF: | AlF3 |
| MW: | 83.98 |
| EINECS: | 232-051-1 |
| Kategorije proizvoda: | metalni halid; Anorganski materijali; Anorganski fluoridi; Aluminijeve soli; Aluminij, metalna i keramička znanost; Kristalni anorganski materijali; Metalna i keramička znanost; Soli |
| Mol datoteka: | 7784-18-1.mol |
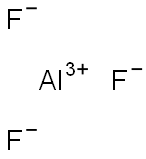 |
|
| Kemijska svojstva aluminijeva fluorida |
| Talište | 1290 stupnjeva (lit.) |
| Vrelište | 1291 stupanj |
| gustoća | 3,1 g/mL na 25 stupnjeva (lit.) |
| Fp | 1250 stupnjeva |
| topljivost | Teško topljiv u kiselinama i alkalijama. Netopljivo u acetonu. |
| oblik | puder |
| boja | Bijela do svijetlo siva |
| Specifična težina | 2.882 |
| Topljivost u vodi | SLABO TOPLJIV |
| Osjetljiv | Higroskopno |
| Sublimacija | 1250 ºC |
| Merck | 14,339 |
| Granice izloženosti | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2 mg/m3; TWA 2,5 mg/m3 |
| Dielektrična konstanta | 2.2 (Ambijentalni) |
| CAS Referenca baze podataka | 7784-18-1(CAS referenca baze podataka) |
| NIST kemijska referenca | Aluminijev trifluorid (7784-18-1) |
| Sustav registra tvari EPA | Aluminijev trifluorid (7784-18-1) |
| Sigurnosne informacije |
| Šifre opasnosti | Xn,T,Xi |
| Izjave o riziku | 22-36/37/38 |
| Izjave o sigurnosti | 26-37/39 |
| RIDADR | 3260 |
| WGK Njemačka | 1 |
| RTECS | BD0725000 |
| Napomena o opasnosti | Vrlo otrovno/nadražujuće |
| TSCA | Da |
| Klasa opasnosti | 8 |
| Grupa za pakiranje | III |
| HS oznaka | 28261210 |
| Podaci o opasnim tvarima | 7784-18-1(Podaci o opasnim tvarima) |
| MSDS informacije |
| Davatelj | Jezik |
|---|---|
| Aluminijev fluorid | engleski |
| SigmaAldrich | engleski |
| ACROS | engleski |
| ALFA | engleski |
| Upotreba i sinteza aluminijevog fluorida |
| Opis | Aluminijev fluorid je u obliku bijele kristalne krutine ili bijelog praha. U prirodi se pojavljuje kao minerali rosenbergite i oskarssonite.1 Može se pripremiti i sintetski. |
| Sinteza | Aluminijev fluorid proizvodi se sljedećim metodama: 1) Fluosilicijeva kiselina s aluminijevim hidroksidom2 H2SiF6 + 2 Al(OH)3 → 2 AlF3 + SiO2 + 4 H2O (I) Reakcija je egzotermna i odvija se u nekoliko koraka. Može se opisati sa sljedeće tri reakcije: 3H2SiF6 + 2 Al(OH)3 → Al2(SiF6)3 + 6 H2O (II) Al2(SiF6)3 + 6 H2O → 2 AlF3 + 3 SiO2 + 12 HF (III) 12 HF + 4 Al(OH)3 → 4 AlF3 + 12 H2O Reakcija se odvija između 70°C i 100°C. Koncentracija fluosilicijeve kiseline može biti čak 35 wt% u vodenoj otopini. Kako je proizvedena otopina aluminijevog fluorida metastabilna i trihidrat počinje brzo kristalizirati na temperaturi od oko 90°C, istaloženi čvrsti silicij mora se ukloniti što je brže moguće. 2) Al2O3 s vodenom otopinom fluorovodične kiseline3 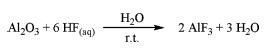 Fluorovodična kiselina je dodana kap po kap uz snažno miješanje na sobnoj temperaturi u suspenziju Al2O3. Nakon toga se čvrsti oksid potpuno otopi. Dobivena bistra otopina se miješa danima na sobnoj temperaturi. Tijekom tog perioda, bijeli kruti precipitat se odvoji od otapala, ispere s vodom i zatim osuši. Nakon obrade u mufelnoj peći na željenoj temperaturi kalcinacije dobiva se aluminijev fluorid. 3) Aluminijev alkoksid s nevodenom otopinom HF4 Aluminijev alkoksid, Al(OR)3 (R=Me, Et, iPr ili tBu), reagira s nevodenom otopinom HF u organskom otapalu. Reakcija se provodi u sol-gel stanju. Nakon starenja nastaje krutina koja se taloži. Krutina je odvojena centrifugiranjem i osušena pod vakuumom. Zatim se primjenjuje fluoriranje osušenog gela u plinskoj fazi kako bi se dobio aluminijev fluorid. |
| Primjena | Aluminijev fluorid jedan je od najvažnijih dodataka u industrijskoj proizvodnji aluminija. Korištenje aluminijevog fluorida može sniziti talište kriolita i poboljšati fizikalna i kemijska svojstva elektrolita. U proizvodnji aluminija, aluminijev oksid se otapa u otopini kriolita. Propuštanjem električne struje kroz otopinu nastaje aluminij. Ipak, otopina kriolita se topi na oko 1000 stupnjeva. Kada se doda aluminijev fluorid, elektroliza se može dogoditi u otopini kriolita na 40-60 stupnju nižoj temperaturi, smanjujući potrebnu količinu energije za proizvodnju aluminija.5 Aluminijev fluorid koristi se kao sloj barijere za usporavanje oksidacije aluminijskih zrcala. 6 Koristi se kao topilo u keramičkim glazurama i emajlima, u proizvodnji aluminijeva silikata i kao katalizator. Kompleksi aluminijevog fluorida s proteinima mogu se koristiti za proučavanje mehaničkih aspekata reakcija prijenosa fosforila u biologiji, koje su od temeljne važnosti jer anhidridi fosforne kiseline kao što su ATP i GTP kontroliraju većinu reakcija uključenih u metabolizam, rast i diferencijaciju.8 Aluminijev fluorid, zajedno s cirkonijevim fluoridom, koristi se za proizvodnju fluoroaluminatnih stakala. U poljoprivredi se aluminijev fluorid može koristiti za sprječavanje fermentacije. Fizički natopljeni aluminijev fluorid može se koristiti kao tanki optički film niskog indeksa u situacijama kada je potrebna daleko UV prozirnost.1 |
| Toksikološke studije | Oralna smrtonosna doza za životinje (LD50) aluminijevog fluorida je 0,1 g/kg. Aluminijev fluorid manje je toksičan od većine fluorida zbog male topljivosti u vodi. Izloženost visokoj koncentraciji aluminijevog fluorida uzrokuje hipokalcijemiju. Udisanje i gutanje aluminijevog fluorida rezultira tipičnim simptomima trovanja fluoridom. Simptomi ozbiljnog trovanja uključuju otežano disanje, kongestiju pluća, mišićni spazam i konvulzije.8 Akutni (kratkoročni) toksični učinci mogu uključivati smrt životinja, ptica ili riba i smrt ili nisku stopu rasta biljaka. Akutni učinci uočavaju se 2 do 4 dana nakon izlaganja životinja ili biljaka aluminijevom fluoridu. Kronični (dugotrajni) toksični učinci mogu uključivati skraćeni životni vijek, reproduktivne probleme, nižu plodnost i promjene u izgledu ili ponašanju kod izloženih životinja. |
| Sigurnosti | Aluminijev fluorid je nezapaljiva krutina. Ali nije kompatibilan s mnogim drugim proizvodima, uključujući kemijski aktivne metale (npr. kalij i natrij), kiseline i kisele pare. Kontakt može izazvati požar ili eksploziju. Prilikom zagrijavanja mogu se emitirati otrovne pare fluorida, uključujući izuzetno otrovni fluorovodik. |
| Reference |
https://en.wikipedia.org/wiki/Aluminij_fluorid John Karlström, Model reaktora za proizvodnju aluminijevog fluorida W. Kleist, C. Häßner, O. Storcheva, K. Köhler, Jednostavna sinteza vodene faze aluminijevog fluorida velike površine i njegove mase i površinske strukture, Inorganica Chimica Acta, 2006, sv. 359, str. 4851-4854 SK Ruediger, U. Groß, M. Feist, H A. Proscott, SC Shekar, SI Troyanov, E. Kemnitz, Mehaničko istraživanje nevodene sinteze aluminijevog fluorida velike površine, Journal of Materials Chemistry, 2005., sv. 15, str. 588-597 https://info.noahtech.com R. Elaish, M. Curioni, K. Gowers, A. Kasuga, H. Habazaki, T. Hashimoto, P. Skeldon, Elelctrochimica Acta, 2017., sv. 245, str. 854-862 Alfred Wittinghofer, Mehanizam signalizacije: Aluminijev fluorid za molekulu godine, 1997., sv. 7, str. R682-R685 Jeffrey Wayne Vincoli, Upravljanje rizikom za opasne kemikalije, Bund 1, 1996., ISBN 1-56670-200-3 |
| Kemijska svojstva | Aluminijev fluorid je bijeli prah ili granula bez mirisa. |
| Kemijska svojstva | Aluminijev fluorid, AlF3, bezvodni je kristalni prah s talištem od 1291 °C. Aluminijev fluorid (hidratizirani), AlF3·31/2H20 je bijeli kristalni prah netopljiv u vodi. |
| Koristi | Proizvodnja aluminija za snižavanje tališta i povećanje vodljivosti elektrolita, topila u keramičkim glazurama i emajlima, proizvodnja aluminijeva silikata, katalizatora. |
| Koristi | Aluminijev fluorid koristi se za proizvodnju metalnog aluminija s niskim talištem, kao topilo u keramičkim glazurama i bijelim emajlima te kao katalizator u kemijskim reakcijama. |
| Koristi | U keramici, kao fluks u metalurgiji, u proizvodnji aluminija, kao inhibitor fermentacije, kao katalizator u organskim reakcijama Aluminijev fluorid koristi se u procesu taljenja za snižavanje tališta elektrolita, proizvodnji aluminijevih silikata, rafiniranju aluminijskih ostataka, proizvodnji specijalnih proizvoda vatrostalni proizvodi, au industriji stakla kao punilo. Koristi se kao sastojak fluksa za uklanjanje magnezija. |
| Opći opis | Bijeli prah ili granule bez mirisa. Gušće od vode. Topivost u vodi na 25 stupnjeva je 0.559 g / 100 mL. |
| Reakcije zraka i vode | Slabo topljiv u vodi |
| Profil reaktivnosti | Aluminijev fluorid kada se zagrijava do uvjeta sublimacije, ispušta otrovne pare fluorida [USCG, 1999]. |
| opasnost | Jako nadražuje tkivo. |
| Opasnost po zdravlje | AKUTNO: iritacija dišnog sustava; moguće krvarenje iz nosa ili povraćanje; KRONIČNO: pogoršava bronhitis/astmu; povećana gustoća kostiju. |
| Opasnost od požara | Posebne opasnosti od proizvoda izgaranja: Kada se zagrijava do uvjeta sublimacije, emitira otrovne pare fluorida |
| Zapaljivost i eksplozivnost | Nije zapaljivo |
| Sigurnosni profil | Otrov gutanjem. Umjereno otrovan supkutanim putem. Jako iritantan za oči. Snažno osjetljiv na udarce u dodiru s Na i K. Kada se zagrijava do raspadanja ispušta otrovne pare F-. Vidi također FLUORIDI i ALUMINIJSKI SPOJEVI. |
| Potencijalno izlaganje | Koristi se kao komponenta elektrolita iz kojeg se proizvodi metalni aluminij; u proizvodnji keramike, emajla, aluminijeva silikata; kao fluks u metalurgiji; kao inhibitor fermentacije |
| Dostava | UN3260 Korozivna krutina, kisela, anorganska, br., Klasa opasnosti: 8; Oznake: 8-Nagrizajući materijal, potreban je tehnički naziv. UN3077 Tvari opasne za okoliš, čvrste, br., Klasa opasnosti: 9; Oznake: 9-Razni opasni materijali, potreban je tehnički naziv. |
| Nekompatibilnosti | Burno reagira s kalijem ili natrijem |
| Zbrinjavanje otpada | Neutralizirati sodom; dodati gašeno vapno; neka odstoji 24 sata. Prijenos mulja u kanalizaciju. |
| Proizvodi i sirovine za pripremu aluminijevog fluorida |
| Sirovine | Sulfuric acid-->Sodium carbonate-->Hydrogen fluoride-->Aluminum hydroxide-->Hexafluorosilicic acid-->Calcium fluoride-->PHOS ROCK FERTILIZER IN BULK-->Methylene Blue trihydrate-->Kremena kiselina |
| Proizvodi za pripremu | Kalijev fluoroaluminat |
Popularni tagovi: aluminij fluorid, Kina aluminij fluorid proizvođači, dobavljači, tvornica
Mogli biste i voljeti
Pošaljite upit


